Новосибирские ученые сделали важное для терапии атеросклероза открытие
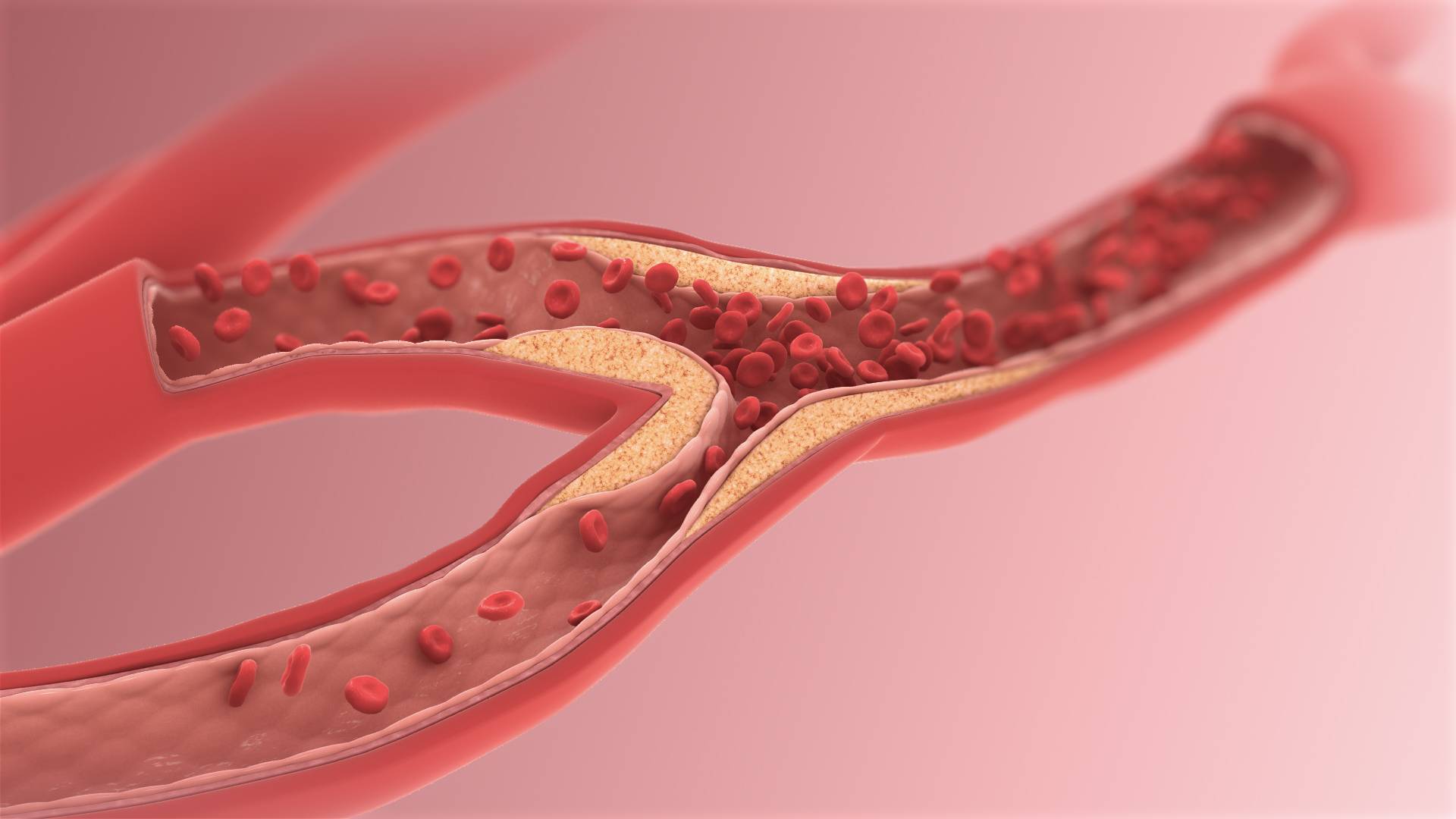
Новые данные о влиянии на организм пациента генетических нарушений, вызывающих семейную гиперхолестеринемию, которые будут использованы в разработках терапии атеросклероза, получили исследователи ФИЦ «Институт цитологии и генетики СО РАН» (ФИЦ ИЦиГ СО РАН), 28 мая сообщает пресс-служба института.
Использование моделей, созданных из клеток реальных пациентов, помогло сотрудникам лаборатории эпигенетики развития ФИЦ ИЦиГ СО РАН установить, что вызывающие семейную гиперхолестеринемию дефекты гена рецепторов липопротеинов низкой плотности (ЛПНП) приводят не только к нарушениям работы клеток печени (что уже было известно), но также и эндотелиальных клеток кровеносных сосудов.
Семейная гиперхолестеринемия (СГХС) является наследственным заболеванием, вызванным генетическим повреждением. Заболевание характеризуется высоким уровнем холестерина крови, что приводит к развитию атеросклероза и вызванных им сердечно-сосудистых заболеваний.
В 85–90% случаев виновниками СГХС становятся нарушения в работе гена рецепторов ЛПНП, которые присутствуют в гетерозиготной форме приблизительно у одного из трехсот человек. То есть группа риска развития этой наследственной болезни велика.
Изучением СГХС совместно с учеными лаборатории эпигенетики развития занимаются сотрудники из НИИ медгенетики Томского национального исследовательского медицинского центра РАН и Московского национального исследовательского медицинского центра кардиологии им. академика Е. И. Чазова.
Исследования ведутся на клеточных моделях, полученных из индуцированных плюрипотентных стволовых клеток (способных к дифференцировке во все типы клеток взрослого организма) реальных пациентов с СГХС.
Предыдущими исследованиями было установлено, что нарушения в гене рецепторов ЛПНП приводят к тому, что клетки печени становятся неспособны улавливать холестерин в нужных объемах. Это приводит к его увеличению в крови с образованием атеросклеротических бляшек, повреждающих внутренний слой кровеносных сосудов — эндотелиальные клетки.
Старший научный сотрудник ФИЦ ИЦиГ СО РАН кандидат биологических наук Ирина Захарова рассказала о полученных ими результатах:
«Мы стали первыми, кто изучал влияние нарушений гена рецепторов ЛПНП на сами эндотелиальные клетки. С помощью клеточной модели пациента мы смогли узнать, что происходит с этими клетками, даже если они не вступали в контакт с атеросклеротической бляшкой, сравнили их с аналогичными клетками здоровых людей. И доказали, что нарушения в работе гена рецепторов ЛПНП сами по себе негативно влияют на клетки сосудов».
Эти результаты, расширив знания о механизмах развития широко распространенного наследственного заболевания, кроме того, имеют и прикладное значение.
Они подтвердили преимущества разработанных в ИЦиГ СО РАН клеточных моделей для подбора эффективной терапии СГХС. Это очень важно потому, что сейчас восстановить нормальные показатели холестерина удается лишь у 3–6% пациентов с гетерозиготной формой заболевания. Увеличить это число можно подбором лекарств, учитывающих класс нарушений в гене (пока их известно пять), а желательно и индивидуальные особенности пациента.
«Животные, в силу различий в метаболизме, плохо подходят для испытаний лекарственных препаратов. Есть свои недостатки и у клеточных моделей, где нарушения в работе гена были созданы искусственно. Наши модели, созданные из клеток реальных пациентов, дают более релевантные результаты, являясь действенным инструментом развития персонифицированной медицины», — пояснила преимущества новых моделей Ирина Захарова.
Ведя дальнейшие исследования эндотелиальных клеток больных СГХС, ученые ИЦиГ продемонстрировали, что CRISPR/Cas-опосредованные методы позволяют редактировать и восстанавливать функциональность клеток.
Геномное редактирование для лечения пациентов с СГХС уже проводится за рубежом. В конце 2023 года начались кинические испытания препарата, исправляющего нарушения в другом гене пациента. Но этот ген отвечает только за 1–2% случаев заболевания.
Однако Ирина Захарова полагает, что использование опыта создания подобных препаратов с учетом результатов исследований ученых ФИЦ ИЦиГ СО РАН имеет хорошие перспективы для разработки новой терапии атеросклероза.
Результаты исследования его участники представили в статье, опубликованной в International Journal of Molecular Sciences.